간세포암(HCC) 치료에 있어 면역 관문 억제제와 항혈관 형성 제제의 병용 요법(Atezolizumab/Bevacizumab)은 표준 치료로 자리 잡았지만, 여전히 상당수의 환자가 치료에 반응하지 않거나 내성을 보입니다. 이러한 저항성의 근본적인 원인을 규명하기 위해 고다마(Kodama) 교수 연구팀은 유전적으로 다양한 마우스 모델과 대규모 임상 데이터를 결합하여, 종양 미세환경을 ‘면역 결핍형(Cold tumor)’으로 만드는 핵심 경로를 찾아냈습니다.
연구의 핵심은 NRF2-COX2-PGE2 신호 전달 축이 종양 내 수지상세포(DC)의 유입을 차단하고 T 세포의 활성을 억제한다는 사실을 밝혀낸 것입니다. 특히 이번 연구는 단순히 현상을 관찰하는 데 그치지 않고, 마우스 모델에서 발견된 발암 유전자 패턴이 실제 인간 환자의 치료 반응성과 어떻게 연결되는지를 다기관 코호트를 통해 입증했다는 점에서 매우 중요한 임상적 가치를 지닙니다.
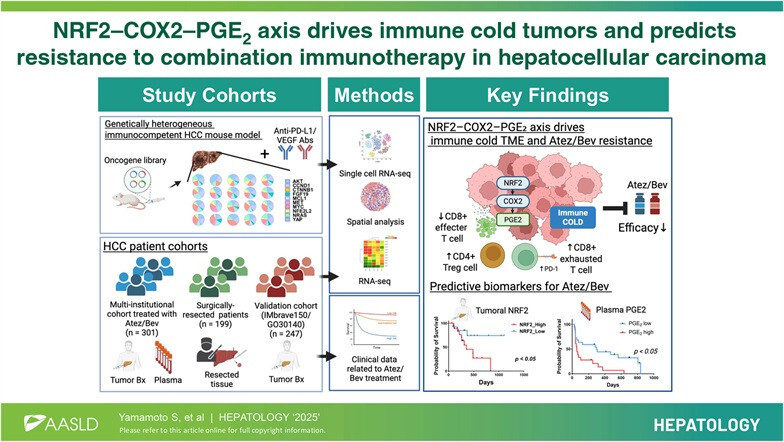
NRF2-COX2-PGE2 축: ‘면역 성벽’을 쌓는 분자 기전
연구팀은 NRF2 신호 경로가 활성화된 종양이 면역 세포의 접근을 원천적으로 차단하는 메커니즘을 규명했습니다.
- NRF2 활성화와 COX2 유도: NFE2L2(NRF2) 유전자가 과발현되거나 돌연변이가 발생하면, 이는 PTGS2(COX2) 유전자의 직접적인 발현 상승으로 이어집니다.
- PGE2의 과분비: COX2에 의해 생성된 프로스타글란딘 E_2(PGE_2)는 종양 미세환경(TME)으로 대량 분비됩니다.
- 면역 세포 유입 차단: 과도한 PGE_2는 종양 내로 들어와야 할 수지상세포의 성숙과 이동을 억제합니다. 수지상세포가 결핍되면 T 세포가 종양을 인식할 수 없게 되어, 결국 면역 관문 억제제가 효과를 발휘하지 못하는 ‘Cold Tumor’ 상태가 됩니다.
연구 방법론: 마우스 모델에서 임상 데이터로의 확장
이번 연구는 실험 모델의 결과가 실제 환자 데이터에서 어떻게 검증되는지를 명확히 보여줍니다.
- 10개 발암 유전자 마우스 모델 (Figure 1): AKT, CCND1, NFE2L2(NRF2) 등 10가지 주요 oncogene을 포함한 라이브러리를 마우스에 주입하여 실제 인간 간암과 유사한 유전적 다양성을 가진 모델을 구축했습니다.
- 내성 유전자 식별: 병용 요법(IO-VEGF) 치료 후에도 살아남은 내성 종양을 분석한 결과, NFE2L2(NRF2) 유전자가 현저하게 농축되어 있음을 확인했습니다.
- 병용 요법의 가능성: NRF2 또는 COX2 억제제를 면역 항암제와 함께 투여했을 때, 막혔던 수지상세포와 T 세포의 유입이 회복되면서 강력한 항종양 효과가 나타났습니다.
분석에 활용된 데이터셋 목록
본 논문은 가설의 입증과 검증을 위해 아래와 같은 방대한 데이터셋을 사용했습니다.
- 마우스 모델 데이터: 10가지 발암 유전자가 포함된 PiggyBac transposon 기반의 내인성 간암 마우스 모델 데이터
- 다기관 치료 레지스트리: Atezolizumab/Bevacizumab 병용 치료를 받은 HCC 환자 코호트 (n=549)
- 수술 절제 코호트: 외과적 절제를 받은 HCC 환자의 유전체 및 임상 데이터 (n=199)
- 외부 임상시험 검증 데이터: IMbrave150 및 GO30140 임상 시험에 등록된 환자들의 RNA-seq 데이터 (n=247)
- 다중 오믹스 데이터: 단일 세포 RNA 시퀀싱(scRNA-seq), 공간 전사체(Spatial transcriptomics), 벌크(Bulk) RNA 시퀀싱 데이터
정리하며
이 연구는 NFE2L2(NRF2) 유전자의 상태가 간암 환자의 면역 항암제 반응성을 예측하는 중요한 바이오마커가 될 수 있음을 시사합니다. 또한, 기존에 널리 사용되던 COX2 억제제(셀레콕시브 등)를 면역 항암제와 병용하는 전략이 ‘Cold Tumor’ 환자들에게 새로운 치료 대안이 될 수 있다는 강력한 근거를 제시했습니다.
이 포스팅이 간암 연구의 최신 동향을 이해하는 데 도움이 되었기를 바랍니다.
